思路迪醫藥聯合開發的皮下注射PD-L1抗體KN035“單藥治療MSI-H/ dMMR晚期實體瘤的Ⅱ期研究結果”獲CSCO展示
2020年09月20日,中國北京,思路迪醫藥宣佈:與江蘇康寧傑瑞生物製藥有限公司(以下簡稱“江蘇康寧傑瑞”)、先聲藥業有限公司(以下簡稱“先聲藥業”)達成戰略合作的新一代PD-L1抗體KN035(通用名:Envafolimab)“單藥治療微衛星高度不穩定(MSI-H)/錯配修復缺陷(dMMR)晚期實體瘤的有效性和安全性的單臂、多中心Ⅱ期研究結果”於CSCO現場公佈,該研究由北京大學腫瘤醫院沈琳教授牽頭並獲今年CSCO優秀論文。
研究題目
Envafolimab(KN035)單藥治療MSI-H/dMMR晚期實體瘤有效性、安全性的單臂、多中心Ⅱ期研究
研究方法
該研究是探索KN035治療MSI-H/dMMR實體瘤的一項關鍵性臨床試驗,採用單臂、多中心研究設計。研究主要終點是獨立評審委員會(BIRC)評估經確認的客觀緩解率(ORR),次要研究終點包括持續緩解時間(DOR)、疾病控制率(DCR)、無進展生存(PFS)和總生存(OS)。結直腸癌(CRC)和胃癌(GC)的MSI-H狀態採用中心實驗室確認,其他腫瘤的MSI-H/dMMR狀態採用當地實驗室確認。
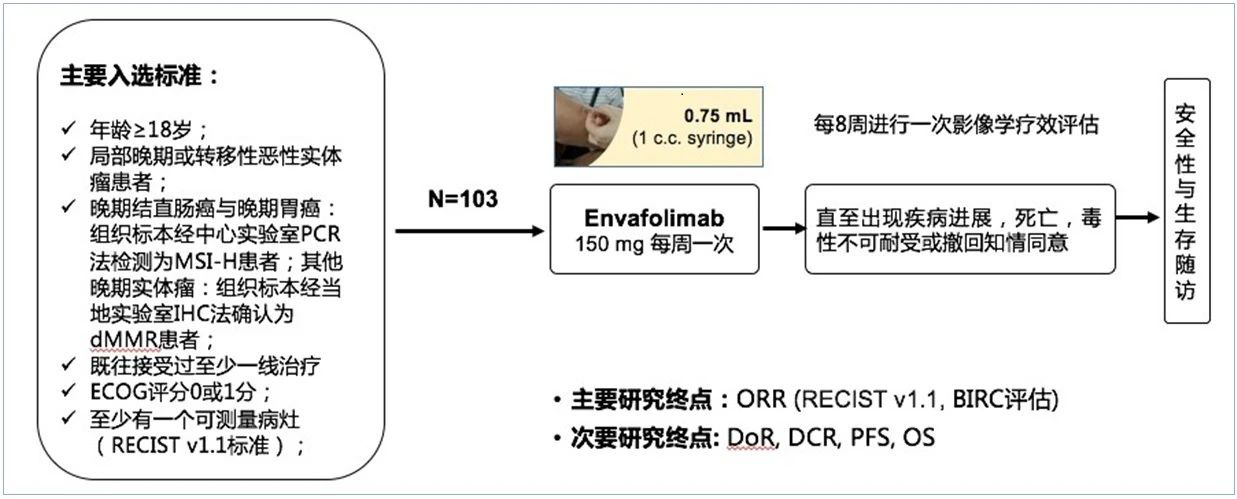
研究結果
發佈的試驗數據截止日期為2020年6月19日,研究共納入103例MSI-H/dMMR晚期癌症患者,其中二/三線經治晚期CRC患者65例,一線及以上經治晚期GC患者18例,一線及以上經治晚期非CRC非GC患者為20例,中比特隨訪時間是11.5個月,最後1例受試者的隨訪時間是6.5個月。所有103例受試者中,55例受試者已終止治療,疾病進展是最主要終止治療原因(67.3%)。
主要亮點
1. KN035單藥治療既往至少一線標準治療失敗的MSI-H/dMMR晚期實體瘤療效顯著,且具有持久性,明顯好於現有治療選擇,與同類產品療效相當:·BIRC評估經確認的ORR在晚期CRC、晚期GC、其他實體瘤和所有人群中分別為43.1%、44.4%、40.0%和42.7%;·中比特DoR均未達到;·中比特OS均未達到,12個月OS率在晚期CRC、晚期GC、其他實體瘤和所有人群中分別為72.9%、83.3%、75.0%和74.6%;

2. KN035具有良好的耐受性和安全性,3-4級TRAE發生率僅為15.5%
3. KN035採用皮下注射給藥,無輸注反應發生,且注射部位反應發生率低;4. 16例患者(15.5%)發生3~4級與藥物相關治療期間不良事件(TEAE)。無研究藥物相關5級TEAE。2.9%的受試者因藥物相關TEAE導致永久停止治療,免疫相關性不良事件發生率和發生情况與同類產品相似,無免疫性肺炎、結直腸炎發生;無輸注反應,注射部位反應發生率8.7%,均是1~2級,無相關嚴重不良事件或導致永久停藥事件發生。

研究結論
KN035可為既往至少一線標準治療失敗的MSI-H/dMMR晚期實體瘤患者帶來全新的安全有效且便利的治療選擇。
參考文獻:沈琳,李健,鄧豔紅等. Envafolimab(KN035)單藥治療MSI-H/dMMR晚期實體瘤的有效性和安全性的單臂、多中心Ⅱ期研究.2020 CSCO年會.
關於思路迪醫藥
思路迪醫藥是一家處於晚期臨床開發及早期商業化佈局階段的生物醫藥公司,秉承“幫助腫瘤患者活得更久更好”的理念,針對腫瘤治療慢病化的未來趨勢,專注為全球癌症患者開發差异化的新一代腫瘤免疫治療藥物,延長腫瘤患者的生存時間,改善患者生活品質。公司產品線包括新一代抗體和小分子抗癌藥物,並擁有一支具有國際化新藥研發、注册和商業化運營能力的團隊。
關於KN035
Envafolimab(KN035)是康寧傑瑞自主研發的PD-L1單域抗體Fc的融合蛋白,基於其獨特設計,在安全性、方便性、依從性方面具有優勢,可用於不適合靜脈輸液的患者,同時具有較低的醫療成本。2016年2月思路迪醫藥與康寧傑瑞達成合作開發協定,康寧傑瑞作為原研方負責生產和質量,思路迪醫藥負責腫瘤領域的全球臨床開發、注册以及商業化階段全球市場開拓和銷售。2020年3月30日,思路迪醫藥、康寧傑瑞、先聲藥業三方達成戰畧合作,康寧傑瑞作為原研方負責生產和質量,思路迪醫藥負責腫瘤領域的全球臨床開發、注册以及境外商業化(1),先聲藥業負責產品在中國大陸的獨家商業推廣。現時Envafolimab(KN035)已在中國、美國和日本針對多個腫瘤適應症同步開展臨床試驗,多個適應症已進入注册/Ⅲ期臨床。Envafolimab(KN035)獲得了美國FDA的晚期膽道癌孤兒藥資格認定,計畫2020年進行中國藥品注册申報。
關於康寧傑瑞
康寧傑瑞生物製藥是一家專注於研發、生產和商業化創新抗腫瘤生物大分子藥物的生物製藥公司。2019年12月12日,公司在香港聯合交易所主機板上市,股票代碼:9966。康寧傑瑞生物製藥在雙特异性抗體及蛋白質工程方面擁有全面整合的研發和製造平臺。公司高度差异化的產品管線由八種腫瘤候選藥物組成,其中六個為全球領先的雙功能抗體,四個產品在中國,美國,日本處於Ⅰ-Ⅲ期臨床試驗開發階段。公司擁有异二聚體及混合抗體等多個具有自主知識產權的科技平臺,以及成熟的符合中國,美國和歐盟cGMP標準的大規模生產能力。公司基於這些國際領先的蛋白質工程平臺打造新一代多功能生物大分子新藥,惠及中國和全球的患者。
關於先聲藥業
先聲藥業是一家快速向創新驅動轉型的公司,聚焦腫瘤、神經、自身免疫等重大疾病領域,獲批建設“轉化醫學與創新藥物國家重點實驗室”,致力於讓患者早日用上更好藥物。憑藉優异的商業化能力,其主要產品在中國保持領先的市場份額。先聲藥業秉持開放式創新的研發策略,與多家跨國藥企成為戰略合作夥伴,促進全球生命科學成果在中國的價值實現。
注:(1)北美地區軟組織肉瘤的臨床開發注册及商業化由Tracon主導
熱門文章

請諮詢我們