恩維達®胃癌和胃食管結合部癌適應症獲孤兒藥資格認定
2025年12月18日,北京,思路迪醫藥(3D Medicines Inc.,股票代碼:1244.HK)宣佈,旗下商業化產品恩維達®(恩沃利單抗注射液)針對胃癌和胃食管結合部癌適應症正式獲得孤兒藥資格認定(Orphan Drug Designation, ODD), 恩維達®繼膽管癌和軟組織肉瘤適應症後成功獲批的第三個孤兒藥適應症。此次獲批基於,本公司開展的恩維達®晚期胃/食管胃結合部腺癌的Ⅱ期臨床研究中已展現出明確的抗腫瘤療效,其聯合FOLFOX方案的客觀緩解率(ORR)達60%,疾病控制率(DCR)高達100%,且安全性與耐受性良好,無導致治療終止或死亡的不良事件发生。
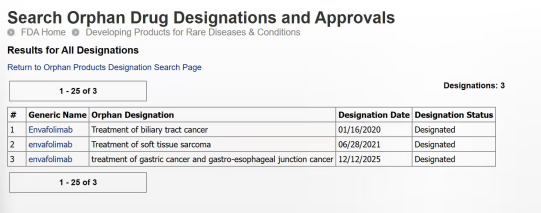
此次孤兒藥資格認定是基於相關監管機構對罕見疾病治療藥物的嚴格評審標準。根據《孤兒藥法案》定義,孤兒藥是用於治療、預防或診斷影響人數較少的罕見疾病的藥物,對於胃癌和胃食管結合部癌適應症這一特定適應症,其適用的患者群體符合罕見疾病的界定要求。獲得該資格認定後,恩維達®在後續的臨床開發與商業化進程中將享有一系列政策支持,包括臨床研究費用稅收減免、藥品獲批後為期7年的市場獨佔權、免除新藥申請相關費用等,這將顯著加速其在該適應症領域的研發推進與市場落地效率。
從臨床價值與市場意義來看,此次獲批具有多重價值。一方面,胃癌作為全球範圍內高發的惡性腫瘤之一,部分亞型患者治療手段有限、預後較差,存在巨大的未被滿足的醫療需求。此次孤兒藥資格的獲批,將推動這一聯合治療方案的進一步研發,為胃癌患者提供更有效的免疫治療選擇。另一方面,這一認定進一步豐富了恩維達®的適應症佈局,為恩維達®的海外授權提供更多機會,銷售預期提供上升空間
恩維達®作為全球首個上市的皮下注射PD-L1抑制劑,憑藉其獨特的分子設計與給藥方式,在有效性、安全性、便利性及依從性上均展現出顯著優勢。與傳統靜脈注射PD-(L)1抗體藥物不同,恩維達®採用皮下注射方式,30秒內即可完成給藥,極大地簡化了治療流程,有效降低了患者就醫頻率與醫療成本,尤其適用於體弱、高齡及存在靜脈輸注反應風險的患者群體。
此次恩維達®胃癌和胃食管結合部癌適應症適應症孤兒藥資格的獲批,是公司在腫瘤治療領域的又一重要里程碑。未來,公司將充分利用孤兒藥相關政策支持,加速推進恩維達®在該適應症領域的臨床研究與商業化進程,同時持續深耕創新藥研發,探索更多腫瘤治療的新方案,為全球腫瘤患者帶來更多希望。
熱門文章

請諮詢我們